 |
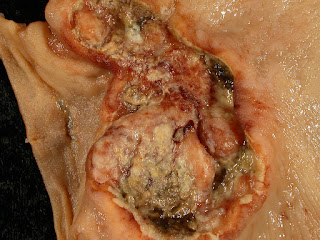
| Adénocarcinome gastrique Source iconographique et légendaire: https://www.flickr.com/photos/euthman/138614039 |
La signalisation et l’angiogénèse médiées par le
VEGF et le VEGF récepteur 2 (VEFGR-2) peuvent contribuer à la pathogénèse et la
progression du cancer gastrique. Notre but était d’évaluer si l’addition de
ramucirumab, un anticorps monoclonal antagoniste du VEFGR-2, à une
chimiothérapie de première ligne, améliore les résultats chez les patients
atteints d’adénocarcinome gastrique ou de la jonction gastro-oesophagienne,
métastasé.
Pour cet essai de phase 3 en double-aveugle,
randomisé, contrôlé par placebo effectué dans 126 centres situés dans 20 pays,
nous avons recruté des patients âgés de 18 ans ou plus, atteints d’adénocarcinome
gastrique ou de la jonction gastro-oesophagienne HER2-négatif, présentant un
statut de rendement ECOG (Eastern Cooperative Oncology Group) de 0 ou 1, et une
fonction adéquate des organes. Les patients éligibles ont été répartis au
hasard (1:1) à l’aide d’un système internet de réponse interactive pour
recevoir cisplatine (80 mg / m2, le premier jour) + capecitabine (1 000 mg / m²,
deux fois par jour pendant 14 jours), tous les 21 jours, + [soit ramucirumab (8 mg/
kg) ou le placebo] aux jours 1 et 8,
tous les 21 jours. L’administration de 5-Fluorouracyle (perfusion de 800 mg /
m² aux jours 1-5) était permise chez les patients dans l’incapacité de prendre
la capecitabine. Le critère principal d’évaluation était la survie sans
progression évaluée par l’investigateur, analysée en intention de traiter chez
les 508 premiers patients. Nous avons effectué une analyse de sensibilité pour
ce qui est du critère principal, incluant une analyse centralisée des examens
de d'imagerie par tomodensitométrie. La survie globale était définie comme critère secondaire de l’étude.
(…).
Entre le 28 janvier 2015 et le 16 septembre 2016,
645 patients étaient répartis au hasard pour recevoir ramucirumab + fluoropyrimidine
et cisplatine (n=326) ou placebo +
fluoropyrimidine et cisplatine (n=319). La survie sans progression, selon l’évaluation
de l’investigateur, était significativement plus longue dans le groupe
ramucirumab par rapport au groupe placebo (hazard ratio [HR] 0.753, Intervalle
de Confiance [IC] 95% 0.607-0.935, p=0.0106 ;
période médiane de survie sans progression 5.7 mois [5.5-6.5] versus 5.4 mois [4.5-5.7]).
Une analyse
de sensibilité basée sur un examen centralisé des images radiologiques par un
comité d’experts indépendant n’a pas corroboré la différence évaluée par l’investigateur
en termes de période de survie sans progression (HR 0.961, IC 95% 0.768-1.203, p=0.74): de fait, il n’y a pas eu de différence
en termes de survie globale entre les groupes (0.962, 0.801-1.156, p=0.6757 ;
médiane de survie globale 11.2 mois [9.9-11.9] dans le groupe ramucirumab versus 10.7 mois [9.5-11.9] dans le
groupe placebo).
Les événements indésirables de grade 3-4 les plus communément
relevés étaient neutropénie (85 [26%] patients sur 323 dans le groupe ramucirumab
versus 85 [27%] patients sur 315 dans le groupe placebo), anémie (39 [12%] versus 44 [14%]), et hypertension (32
[10%] versus 5 [2%]).
L’incidence des événements indésirables graves, quelqu’en
soit le grade, était de 160 (50%) patients atteints sur 323 dans le groupe ramucirumab
et de 149 (47%) patients atteints sur 315 dans le groupe placebo. Les événements
indésirables graves les plus communément relevés étaient vomissement (14 [4%]
dans le groupe ramucirumab versus 21 [7%] dans le groupe placebo) et diarrhée (11
[3%] versus 19 [6%]). Sept décès ont été dénombrés dans chaque groupe, soit
pendant la période d’administration du traitement à l’étude, ou soit dans les
30 jours après interruption du traitement à l’étude, conséquents à des événements
indésirables liés au traitement. (…).
Bien que l’analyse principale de survie sans
progression était statistiquement significative, ce résultat n’était pas confirmé
par l’analyse de sensibilité de survie sans progression réalisée par un comité
d’experts indépendant ; ledit résultat n’ayant pas amélioré la survie
globale. Par conséquent, l’addition de ramucirumab au traitement [cisplatine + chimiothérapie
fluoropyrimidine n’est pas à recommander comme traitement de première ligne
pour cette population de patients. Charles S Fuchs, MD, et al, dans The Lancet Oncology, publication en ligne en avant-première, 1er février 2019
Financement :
Eli Lilly and Company
Source :
The Lancet Online / Traduction et adaptation : NZ
Aucun commentaire:
Enregistrer un commentaire