|
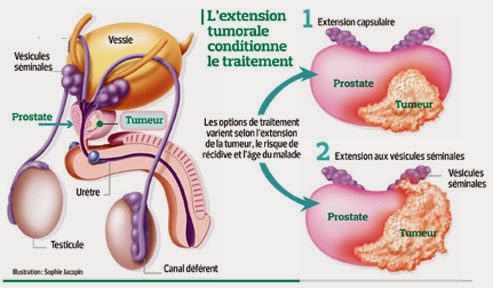
| Prostate et vésicules séminales normales. Source iconographique et légendaire:https://fr.wikipedia.org/wiki/Cancer_de_la_prostate |
La durée optimale de la privation androgénique associée à une radiothérapie à haute dose dans le cancer de la prostate reste controversée. L'essai DART 01/05 a été conçu pour déterminer si la privation androgénique à long terme est supérieure à la privation androgénique à court terme lorsqu'elle est associée à une radiothérapie à haute dose. Les résultats à 5 ans ont montré que 2 ans de privation androgénique adjuvante associée à une radiothérapie à haute dose amélioraient significativement le contrôle biochimique, les métastases et la survie globale, en particulier chez les patients atteints d'une maladie à haut risque. Dans ce rapport, nous présentons les résultats finaux de l'essai sur 10 ans.
Cet essai ouvert, de phase 3, randomisé et contrôlé a été réalisé dans dix hôpitaux en Espagne. Les critères d'éligibilité incluaient les patients âgés de 18 ans ou plus atteints d'un adénocarcinome de la prostate histologiquement confirmé de stade clinique T1c à T3, N0 et M0, selon la classification de 2002 de l'American Joint Committee on Cancer, avec des facteurs de risque intermédiaire et de risque élevé, un taux d’antigène spécifique de la prostate (PSA) inférieur à 100 ng/mL, et un score de performance de Karnofsky d'au moins 70 %. Les patients ont été randomisés (1:1) pour recevoir 4 mois de traitement néoadjuvant et concomitant de privation androgénique à court terme (STAD) plus une radiothérapie à haute dose (dose minimale 76 Gy ; dose médiane 78 Gy) ou pour recevoir le même traitement suivi de 24 mois de privation androgénique à long terme (DLTA) adjuvante, via un programme de randomisation généré par le logiciel d'analyse statistique (version 9.1) et un système de réponse Web interactif. Les patients assignés au groupe STAD ont reçu 4 mois de privation androgénique néoadjuvante et concomitante (flutamide oral 750 mg par jour ou bicalutamide oral 50 mg par jour) avec de la goséréline sous-cutanée (2 mois avant et 2 mois en association avec une radiothérapie à forte dose). Un traitement anti-androgène a été ajouté au cours des 2 premiers mois de traitement. Les patients assignés au DLTA ont continué avec la goséréline tous les 3 mois pendant 24 mois supplémentaires. Le critère principal était la survie sans maladie biochimique à 5 ans. Pour cette étude de 10 ans, nous avons analysé la survie globale, la survie sans métastase, la survie sans maladie biochimique et la survie par cause. L'analyse a été faite dans le but de traiter. Cet essai est clos. (…).
Entre le 7 novembre 2005 et le 20 décembre 2010, 355 patients ont été recrutés. Un patient du groupe STAD s'est retiré de l'essai, donc 354 participants ont été assignés au hasard au groupe STAD (n = 177) ou au groupe DLTA (n = 177). Le suivi médian était de 119·4 mois (Intervalle Interquartile [IQR] 100,6–124,3). La survie sans maladie biochimique à 10 ans pour le groupe DLTA était de 70,2 % (Intervalle de Confiance [IC] à 95 % 63,1–77,3) ; et pour le groupe STAD, elle était de 62,3 % (54,9–69,7 ; risque relatif [HR] 0,84 ; IC à 95 % 0,50–1,43 ; p = 0,52). À 10 ans, la survie globale était de 78,4 % (72,1–84,8) pour le DLTA et de 73,3 % (66,6–80,0) pour le groupe STAD (HR 0,84 ; IC à 95 % 0,55 –1,27 ; p=0,40), et la survie sans métastase était de 76,0 % (69,4–82,7) pour le groupe DLTA et de 70,9 % (64,0–77,8) pour le groupe STAD (HR 0,90 ; IC à 95 %, 0,37–2,19 ; p = 0,81). Pour le sous-groupe de patients à haut risque, la survie sans maladie biochimique à 10 ans était de 67,2 % (57,2–77,2) pour le groupe DLTA et de 53,7 % (43,3–64,1) pour le groupe STAD (HR 0,90 ; IC 95 % 0,49–1,64 ; p=0·73) ; la survie globale à 10 ans était de 78,5 % (69,6–87,3) pour le groupe DLTA et de 67,0 % (57,3–76,7) pour le groupe STAD (HR 0,58 ; IC 95 % 0,33–1,01 ; p=0·054) ; et la survie sans métastase à 10 ans était de 76,6 % (IC 95 % 67,6–85,6) pour le DLTA et 65,0 % (55,1–74,8) pour le STAD (HR 0,89 ; IC 95 % 0,33–2,43 ; p=0,82). Seuls 11 (3%) des 354 patients sont décédés du cancer de la prostate, tous dans le sous-groupe à haut risque (cinq dans le groupe DLTA et six dans le groupe STAD). 76 (21%) patients sont décédés d'autres causes (principalement des seconds cancers chez 31 [9%] patients et des maladies cardiovasculaires chez 21 patients [6%]). Aucun décès lié au traitement n'a été observé.
Après un suivi prolongé de 10 ans, nous n'avons pas été en mesure de soutenir le bénéfice significatif du protocole DLTA rapporté à 5 ans. Cependant, l'ampleur du bénéfice était cliniquement pertinente chez les patients à haut risque. Les patients à risque intermédiaire traités par radiothérapie à haute dose ne bénéficient pas du DLTA. Une caractérisation biologique avec l'inclusion de tests génomiques est nécessaire dans le processus de prise de décision. Almuneda Zapatero, PhD, et al, dans The Lancet Oncology, publication en ligne en avant-première, 12 avril 2022
Financement : Groupe de Recherche en Oncologie Radiothérapique et Société Espagnole d’Oncologie Radiothérapique, Agence d’Etat de la Recherche, Astra Zeneca
Source : The
Lancet Online / Préparation post : NZ